Sinopharm (Pekin): BBIBP-CorV
Faza 1
1 Gjyqi
ChiCTR2000032459
Kina
Faza 2
2 gjyqe
NCT04962906
Argjentina
ChiCTR2000032459
Kina
FAZA 3
6 gjyqe
NCT04984408
ChiCTR2000034780
Emiratet e Bashkuara Arabe
NCT04612972
Peru
NCT04510207
Bahreini, Egjipti, Jordania, Emiratet e Bashkuara Arabe
NCT04560881, BIBP2020003AR
Argjentina
NCT04917523
Emiratet e Bashkuara Arabe
Miratimet
Lista e Përdorimit të Emergjencave të OBSH -së 59 vende
Angola 、 Argjentina 、 Bahreini 、 Bangladeshi 、 Bjellorusia 、 Belize 、 Bolivia (Shteti Plurinacional i) 、 Brazili 、 Brunei Darussalam 、 Kamboxhia 、 Kameruni 、 Çad 、 Kina 、 Komoret 、 Egjipti Gu Guinea Ekuatoriale 、 Gabon 、 Gambia 、 Gjeorgji 、 Gjeorgji 、 Guiani 、 Gjeorgji 、 、 Iran (Republika Islamike e) 、 Irak 、 Jordan 、 Kirgistan 、 Republika Demokratike Popullore Lao
Liban 、 Malajzi 、 Maldive 、 Mauritania 、 auritius 、 Mongolia 、 Mali i Zi 、 Marok 、 Mozambik 、 Namibia 、 Nepal 、 Niger Macedonia Maqedonia e Veriut 、 Pakistan 、 Paraguaj 、 Peru 、 Filipine 、 Republika e Kongos 、 Sieragon les Serie 、 Serbi Ishujt 、 Somali 、 Sri Lanka 、 Tajlandë 、 Trinidad dhe Tobago 、 Tunizi Em Emiratet e Bashkuara Arabe 、 Venezuela (Republika Bolivariane e) 、 Vietnam 、 Zimbabve
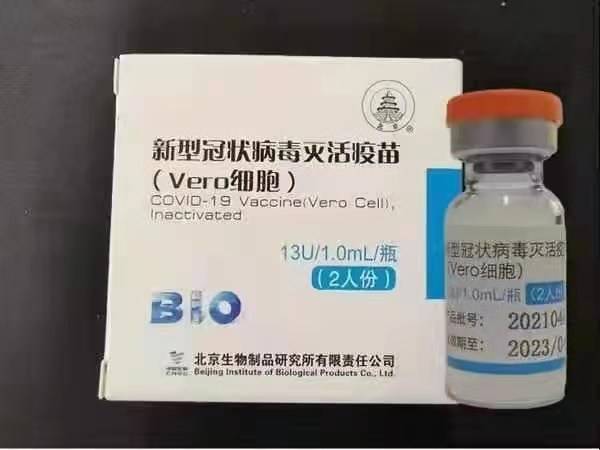
Sinopharm BBIBP-CorV COVID-19 është një vaksinë e çaktivizuar e bërë nga grimca virusi të kultivuara që nuk kanë aftësi patogjene. Ky kandidat për vaksinë u zhvillua nga Sinopharm Holdings dhe Instituti i Produkteve Biologjike në Pekin.
Vaksina Sinopharm BBIBP-CorV funksionon duke lejuar sistemin imunitar të prodhojë antitrupa kundër koronavirusit beta SARS-CoV-2. Vaksinat e virusit të çaktivizuara janë përdorur për dekada të tëra, të tilla si vaksina e tërbimit dhe vaksina e hepatitit A. Kjo teknologji zhvillimi është aplikuar me sukses në shumë vaksina të njohura, siç është vaksina e tërbimit.
Lloji SARS-CoV-2 i Sinopharm (lloji WIV04 dhe numri i bibliotekës MN996528) u izolua nga një pacient në Spitalin Jinyintan në Wuhan, Kinë. Virusi u përhap në kulturë në një linjë qelizore kompetente Vero, dhe supernatanti i qelizave të infektuara u çaktivizua me β-propiolakton (1: 4000 vol/vol, 2 deri në 8 ° C) për 48 orë. Pas sqarimit të mbeturinave të qelizave dhe ultrafiltrimit, një çaktivizim i dytë β-propiolactone u krye në të njëjtat kushte si çaktivizimi i parë. Sipas OBSH-së, vaksina u absorbua në 0.5 mg alum dhe u ngarkua në shiringa të para-mbushura në 0.5 ml kripur steril të zbutur me fosfat pa konservantë.
Më 31 Dhjetor 2020, Administrata Shtetërore e Barnave njoftoi miratimin e vaksinës eksperimentale të zhvilluar nga Sinopharm.
Më 7 maj 2021, Organizata Botërore e Shëndetit njoftoi miratimin e vaksinës. Lista e përdorimit urgjent të OBSH-së u mundësoi vendeve të përshpejtojnë miratimet e tyre rregullatore për të importuar dhe administruar vaksinën COVID-19. Grupi i Ekspertëve Këshillues të OBSH -së për Strategjitë e Imunizimit gjithashtu ka përfunduar rishikimin e tij të vaksinës. Bazuar në të gjitha dëshmitë në dispozicion, OBSH rekomandon dy doza të vaksinës, tre deri në katër javë, për të rriturit 18 vjeç e lart. Efikasiteti i vaksinës kundër sëmundjeve simptomatike dhe të shtruara në spital vlerësohet në 79% për të gjitha grupmoshat e kombinuara.
Shoqata Mjekësore Amerikane botoi "Një Provë Klinike e Randomizuar: Efekti i 2 Vaksinave të Inaktivizuara SARS-CoV-2 në Infeksionin Simptomatik COVID-19 tek të Rriturit" më 26 maj 2021, duke arritur në përfundimin se "në këtë analizë të paracaktuar të ndërmjetme të një prove klinike të rastit, të rriturit 2 vaksinat e paaktivizuara SARS-CoV-2 të administruara në këtë analizë të paracaktuar të ndërmjetme të provave klinike të rastësishme ulën ndjeshëm rrezikun e simptomave COVID-19, dhe ngjarje të rënda negative ishin të rralla. " Në këtë fazë të testimit të rastit 3 në të rriturit, efikasiteti i 2 vaksinave të çaktivizuara të të gjithë virusit në rastet simptomatike të COVID-19 ishte 72.8% dhe 78.1%, respektivisht. 2 vaksina kishin ngjarje të rralla serioze negative me frekuencë të ngjashme me grupin e kontrollit vetëm për shap, dhe shumica nuk kishin lidhje me vaksinimin. Një analizë eksploruese zbuloi se 2 vaksinat shkaktuan antitrupa neutralizues të matshëm, të ngjashëm me rezultatet e provës së fazës 1/2.
Grupi i Punës i WHO SAGE publikoi një përmbledhje të vaksinës Sinopharm/BBIBP COVID-19 më 10 maj 2021. Vaksina COVID-19 e GAVI përfshin një monitor shishkë vaksine që u tregon punonjësve shëndetësorë nëse vaksina është ruajtur siç duhet dhe nuk është ekspozuar ndaj mbinxehje. Si rezultat, dëmtimi, raportoi GAVI më 14 maj 2021. etiketat inteligjente të prodhuara nga Zebra Technologies dhe të bëra nga Temptime Corporation, përbëhen nga një rreth me një katror me ngjyrë më të lehtë në mes, të bërë nga një kimikat pa ngjyrë që zhvillon në mënyrë të pakthyeshme ngjyrën me kalimin e kohës Me Kjo bëhet më e errët për të dhënë një tregues vizual të ekspozimit kumulativ të nxehtësisë. Pasi shishka është ekspozuar ndaj nxehtësisë përtej intervalit të saj optimal të ruajtjes, sheshi bëhet më i errët se rrethi, duke treguar se vaksina nuk duhet të përdoret më.
Numri i regjistrimit të bibliotekës së ilaçeve të vaksinave kundër drogës BBIBP-CorV COVID-19: DB15807.